安徽省重点水域水生生物资源监测项目浮游动物样品采集分析与保存工作规程
浮游动物样品采集参照《长江水生生物资源监测手册》(中国农业出版社,2021年)、《内陆水域渔业自然资源调查手册》(农业出版社,1991年)、《河流水生生物调查指南》(科学出版社,2014年)、《水生态监测技术要求淡水浮游动物(试行)》(总站水字﹝2022﹞47号),鉴定分析参照《微型生物监测新技术》(中国建筑工业出版社,1990年)、《中国淡水轮虫志》(科学出版社,1961年)、《中国典型地带轮虫的研究》(学位论文,1997年)、《中国动物志 节肢动物门 甲壳纲 淡水枝角类》(科学出版社,1979年)、《长江流域的枝角类》(中国科学技术出版社,2015年)、《中国动物志 节肢动物门 甲壳纲 淡水桡足类》(科学出版社,1979年)等。
一、主要材料
1. 主要工具
25号浮游生物网:网孔直径为0.064 mm,网呈圆锥形,网口套在环上,网底端有出水开关活塞。
定性样品瓶:100 mL样品瓶。
采水器:采水器为圆柱形,上下底面均有活门。采水器沉入水中,活门可自动打开。容量和深度规格要满足采样要求,容量可为1 L和5 L。
定量样品瓶:1 L样品瓶和100 mL样品瓶。
塑料水桶。
浓缩装置:1 L具刻度直型漏斗和铁架台,直型漏斗100 mL处有标记。
虹吸装置:由吸耳球、虹吸软管、硬质玻璃管或塑料管组成,玻璃管前端以筛绢封口。
载玻片:26 mm×76 mm。
盖玻片:22 mm×22 mm;24 mm×24 mm;24 mm×75 mm。
正置显微镜:物镜4×、10×、20×、40×、100×;目镜10×或15×,带摄影系统。
体视显微镜:物镜0.8×或1.0×,可调变倍比≥4:1,目镜10×或15×,带摄影系统。
浮游生物计数框:1 mL及5 mL定量计数框。1 mL框的内框50 mm×20 mm,横竖划分为10×4行,共40个计数小格,每个计数小格内框为5 mm×5 mm。5 mL定量计数框为S型。
移液枪:1 mL和5 mL移液枪。
计数器。
2. 试剂
鲁哥氏液:称取60 g碘化钾溶于100 mL蒸馏水中,待完全溶解后加入40 g碘,充分摇动至碘完全溶解,加蒸馏水定容至1000 mL,贮存于棕色磨口玻璃瓶。鲁哥氏液在室温避光条件下保存。
甲醛溶液:w(HCHO)=37%~40%。
二、样品采集
1. 浮游动物分层采样应满足以下要求
①水深<3 m时,在中层(1/2水深处)布设1个采样点;
②3 m≤水深<6 m时,在表层(水面下0.5 m处)和底层(底泥界面以上0.5 m处)各布设1个采样点,水样等比例混合备用;
③6 m≤水深≤10 m时,分别在表层、中层和底层各布设1个采样点,水样等比例混合备用;
④水深>10 m时,分别在表层、5 m和10 m处布设1个采样点,水样等比例混合备用,10 m以下区域除特殊需要一般不采样。
2. 采样频次
繁殖期(4-7月)、索饵期(9-11月)各开展1次。
3. 原生动物和轮虫定量样品采集
根据水深分层采样,将各层水样等量混匀后,取1 L水样至1 L带刻度的样品瓶中,加入鲁哥氏液(用量为水样体积的1.5%,即1000 mL水样加15 mL鲁哥氏液)固定,作为原生动物和轮虫定量样品。
4. 枝角类和桡足类定量样品采集
取20 L混合均匀的水样,通过13号浮游生物网过滤浓缩至100 mL样品瓶中,并加入鲁哥氏液(用量为水样体积的1.5%)固定,作为枝角类和桡足类定量样品。
5. 浮游动物定性样品采集
拖动25号浮游生物网在水体表层做“∞”形往复约3~5 min,然后将浮游生物网缓慢提出水面,将网底部收集管中样品转移至100 mL样品瓶中,加入甲醛溶液(用量为水样体积的5%)固定,作为浮游动物定性样品。
注:每个站位于不同生境采集的定性样品混合为1份样品,标注该站位编号。
6. 样品编码
定量样品编码方式采用“监测站位+采样点位(每个监测站位设置3个采样点位)+原生动物、轮虫定量/枝角类、桡足类定量(简称原轮定量/枝桡定量)+采样年月日”(如站位1-1-原轮定量-2023/4/1,表示2023年4月1日采集1号监测站位1号采样点原生动物、轮虫定量样品;站位1-1-枝桡定量-2023/4/1,表示2023年4月1日采集1号监测站位1号采样点桡足类、枝角类定量样品)。
定性样品编码方式采用“监测站位+浮游动物定性(简称浮动定性)+采样年月日”(如1-浮动定性-2023/4/1,表示2023年4月1日采集1号监测站位浮游动物定性样品)。
三、沉淀浓缩
将每个采样点的原生动物和轮虫定量样品分别缓慢倒入浓缩装置中,室温静置48 h及以上进行第一次沉降浓缩,旋开浓缩装置底部活塞,将沉淀物收集在100 mL样品瓶中,再用5 mL移液枪吸取5 mL上清液冲洗浓缩装置1次,将冲洗水一并收集在100 mL样品瓶中,然后再次室温静置48 h以上进行二次沉降浓缩,用1 mL移液枪吸取上清液,直至沉淀物处于100 mL标记线。静置初期,应适时轻敲浓缩装置器壁减少吸附。
注:样品也可在原样品瓶中直接浓缩,用虹吸装置缓慢吸取上清液,直至沉淀物处于100 mL标记线,具体操作步骤与浓缩装置同上。虹吸过程中,吸液口与浮游动物沉淀物间距离应大于3 cm。
枝角类、桡足类定量样品无需进行此前处理。可以直接用于鉴定。
四、样品寄送
样品采集后需在5日内完成定性和定量样品送样,每个站位寄送浮游动物样品7瓶,分别为1瓶浮游动物定性样品(简称浮动定性)、3瓶原生动物和轮虫定量样品(简称原轮定量)、3瓶枝角类和桡足类定量样品(简称枝桡定量)。样品瓶应确保严格密封,同时发送寄样清单至鉴定人员,核对样品数量、样品编码等信息。寄样清单格式:
|
序号 |
送样 日期 |
分项 报告 |
采样 站位 |
送样人 |
采样 日期 |
类别 |
采样 体积 |
浓缩 体积 |
样品 数量 |
样品编号 |
|
1 |
2023/4/6 |
长江安徽段 |
站位1 |
张三 电话: |
2023/4/1 |
浮游动物定性样品 |
不需填报 |
不需填报 |
1 |
站位1-浮动定性-2023/4/1 |
|
原生动物与轮虫定量样品 |
1L |
100mL |
3 |
站位1-1/2/3-原轮定量-2023/4/1 |
||||||
|
枝角类和桡足类定量样品 |
20L |
不需填报 |
3 |
站位1-1/2/3-枝桡定量-2023/4/1 |
||||||
|
2 |
2023/4/6 |
长江安徽段 |
站位2 |
张三 电话: |
2023/4/1 |
浮游动物定性样品 |
不需填报 |
不需填报 |
1 |
站位2-浮动定性-2023/4/1 |
|
原生动物与轮虫定量样品 |
1L |
100mL |
3 |
站位2-1/2/3-原轮定量-2023/4/1 |
||||||
|
枝角类和桡足类定量样品 |
20L |
不需填报 |
3 |
站位2-1/2/3-枝桡定量-2023/4/1 |
五、样品鉴定分析
1. 定量分析
①原生动物和轮虫
将浓缩样品充分混匀,用移液器准确吸取1 mL样品,置于1 mL浮游生物计数框内,分别在正置显微镜10×或40×下全片计数轮虫和原生动物。每一样品需平行计数2次,取平均值,每次计数结果与其平均值之差应不大于15%,否则应增加计数1次,直至有两次计数结果符合要求为止。
②枝角类和桡足类
用移液器准确吸取5 mL样品,置于5 mL浮游生物计数框内,在正置显微镜4×或10×下将20 L样品浓缩过滤物中甲壳动物分若干次全部计数。或将样品静置4 h,经初步沉淀浓缩(至50 mL以下)、二次沉淀浓缩(第一次沉淀浓缩样品转移至100 mL样品瓶中静置4 h后进行),最终定容至10 mL,两次沉淀后移除的上清液应保留并置于正置显微镜下镜检有无遗漏生物体(如有,应计入枝角类和桡足类生物量)。枝角类和桡足类样品一般需要全样计数,如个别样品中个体数量太多,可视情吸取一定量样品进行镜检,一般应确保抽样计数个体数大于300个。
残体以头部或尾部计数,同一种类(或同一态)的残体只能按其中一种方法计数,以数量较多者为准。
2. 定性分析
定性样品取样前不需要摇匀,原生动物和轮虫定性样品鉴定时使用吸管从瓶底吸取约1 mL样品放于1 mL计数框中,在正置显微镜物镜10×(轮虫)和40×(轮虫、原生动物)下观察鉴定,每个定性样品观察不少于2 mL。鉴定困难的原生动物和轮虫物种需单独吸取至载玻片上,加盖玻片后于油镜下观察鉴定。枝角类和桡足类样品鉴定时从瓶底吸取约5 mL样品放于5 mL计数框中,在正置显微镜下观察鉴定,对于密度较低的样品,需要全瓶观察。难以鉴定的枝角类和桡足类物种需要用吸管吸取到盖玻片上,在体视剖镜下用解剖针解剖关键部位(如第五对胸足)进行鉴定观察。对于密度较高或杂质较多的样品,需要稀释后再进行物种鉴定。
3. 分析记录
浮游动物定量和定性样品分析记录表格式,见附录。
4. 密度和生物量计算
①按下式换算原生动物和轮虫的密度:
N=(Vs×n)/(V×Va)
式中:N为1 L水中原生动物和轮虫的个体数(ind./L);V为采样体积(L);Vs为沉淀体积(mL);Va为抽样体积(mL);n为抽样计数所得的个体数。
②浮游动物生物量计算方法如下:
原生动物、轮虫生物量可采用体积法求得生物体积,比重取1,再根据体积换算为生物量。原生动物测量体长和体宽,然后分别求出平均值,按公式1计算出近似体积。轮虫测量长度和宽度按照淡水常见轮虫近似求积公式计算公式(章宗涉和黄祥飞,1991)。枝角类和桡足类利用体长-体重回归方程(公式2),由体长计算体重(湿重)。无节幼体按照0.003mg/个计算。长度测量时,通过对每个种类随机选取30个不同大小的个体进行测量体长,其中枝角类测量从头部顶端(不含头盔)至壳刺基部的长度,桡足类测量从头部顶端至尾叉末端的长度,最后取平均值得到每种的体长。对于数量少于30个的种类,尽可能全部测量。
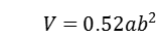 公式1
公式1
式1中V为原生动物体积,单位是立方微米(μm3),a是体长,单位为微米(μm),b是体宽,单位为微米(μm)。公式参考《湖泊水生态监测规范》(DB 32/T 3202—2017)。
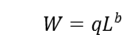 公式2
公式2
式2中W为生物量,单位微克(μg),L为体长微米(μm),q、b为系数,不同类群系数的值参考《淡水浮游生物研究方法》(章宗涉和黄祥飞,1991)。
六、样品保存
已固定而未完成鉴定的样品在室温避光条件下保存,保存时间不超过3个月;1℃~5℃冷藏避光条件下可保存12个月。样品在保存过程中,应每周检查鲁哥氏液的氧化程度,如果样品颜色变浅,应向样品中补加适量的鲁哥氏液,直至样品颜色恢复为黄褐色。
完成鉴定分析后的样品,应加入甲醛溶液(用量为水样体积的5%),以长期保存样品。所有样品鉴定完成后,需将样品送回中国水产科学研究院淡水渔业研究中心保存。
附录
浮游动物样品分析记录表
采集地点: 定性/定量:
采样体积: 浓缩体积: 固定剂:
鉴定人员:
|
样品采集日期 |
鉴定日期 |
样品编号 |
物种名称 |
第1片P1 |
第2片P2 |
第3片P3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 皖公网安备 34152302000043号
皖公网安备 34152302000043号